近日,beat365官方网站應用化學系劉志博團隊在ACS Central Science期刊發表題為“Targeted Radionuclide Therapy Activates Prodrugs for Treating Metastasis”的論文,本研究揭示了常見的醫用β核素驅動前藥釋放的潛力,并以[177Lu]Lu為例開發了鉑(IV)前藥的激活體系,應用于轉移瘤的聯合治療,為靶向放射性核素治療與化療結合的提供新範式。
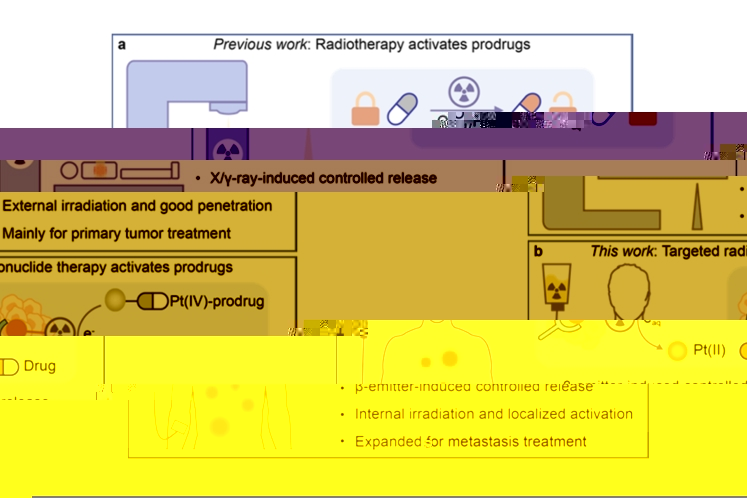
圖1 靶向放射性核素治療示意圖
超過60%的癌症患者接受放化療聯合治療,但化療藥物的毒副作用和放療總劑量限制阻礙了該策略在臨床上的更廣泛應用。近年來,基于水輻解産生的活性粒子,研究者們開發了适用于小分子、抗體偶聯藥物(ADC)及納米框架的放療射線驅動的前藥釋放體系,在腫瘤處精準激活化療藥物,實現放化療聯合的“降毒增效”。
從臨床實際出發,超過90%的癌症患者因轉移而死亡,外源放療作為局部治療手段,難以有效幹預轉移性腫瘤,無法阻止其進一步惡化。因此,開發新型輻射驅動的前藥激活策略,以應對轉移性腫瘤的治療需求,成為推動該領域發展的關鍵挑戰之一。靶向放射性核素治療作為一種新興治療模式,憑借其在療效和安全性方面的顯著潛力,為轉移性腫瘤的治療帶來了新的希望。
在放療激活前藥研究的基礎上,該研究聚焦在臨床常用放射性核素([18F]F,[68Ga]Ga, [86Y]Y, [89Zr]Zr, [177Lu]Lu等)發射的β射線驅動鉑(IV)前藥激活的潛力。研究表明,幾種常見的醫用β核素均能驅動鉑(IV)前藥軸向配體的釋放,且反應速率和效率與放射性核素的半衰期和衰變能量密切相關。通過Geant4模拟評估不同放射性核素沉積能量随時間的變化,結果顯示鉑(IV)前藥的激活效率與沉積能量呈線性關系。這一發現表明,通過模拟放射性核素的沉積劑量,可以預測前藥激活反應的效率。
為進一步闡明該反應的應用場景,作者設計了一種以治療型核素Lu-177為激活劑的鉑(IV)前藥系統。該策略能夠在腫瘤局部實現高效激活,有效抑制荷瘤小鼠的皮下和轉移性腫瘤生長。研究揭示了放射性核素内照射驅動反應的潛力,搭建了外源射線誘導反應與放射性藥物内照射之間的橋梁,并為放射性藥物與化療、免疫治療策略的結合提供了新的思路,有望解決癌症轉移等臨床難題。
beat365官方网站劉志博教授為該論文通訊作者,beat365官方网站博士研究生郭志濱為論文第一作者。該工作得到了beat365官方网站、北大-清華生命科學聯合中心、昌平實驗室、北京分子科學國家研究中心、中華人民共和國科學技術部、國家傑出青年科學基金、北京市自然科學基金的資助。
原文鍊接:https://pubs.acs.org/doi/10.1021/acscentsci.4c01369
排版:高楊
審核:牛林,楊四海